有機化学のオキテ7,8
問題
化合物AおよびBは,アルケン(エチレン系炭化水素)に属する化合物である。化合物A,Bを燃焼させて元素分析したところ,いずれもその質量割合はC=85.7(%)とH=14.3(%)であった。化合物A,およびBそれぞれに臭素水を加えて振ると付加反応が起り,直ちに臭素水の褐色が消えて透明に変化し,その付加物の分子量はいずれも216であった。化合物AとBの混合物1.0molを①ある酸化剤を用いて酸化すると,アルデヒドとケトンが生成した。得られたアルデヒドの総生成量は1.5molであり,そのうちの1.0molはホルムアルデヒドであり,残りのアルデヒドは0.50molであった。一方,ケトンの生成量は0.50molであり,このケトンに水酸化ナトリウム水溶液とヨウ素を加えて加熱したところ,②黄色結晶の沈殿物が得られた。なお,本実験で用いた酸化剤によるアルケンの酸化反応式を下記に示す。式中のR1,R2,R3,およびR4は,水素,またはアルキル基である。
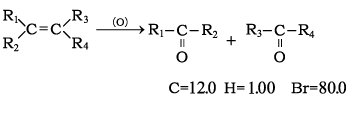
- 【問1】化合物A,およびBの分子式を記せ。
- 【問2】下線部①の酸化反応式で得られるケトンの構造式(示性式)を記せ。
- 【問3】本実験で用いた混合物1.0mol中に含まれるアルケン化合物AとBの物質量の比(A:B)をa)~e)の中から一つ選びなさい。
- a)1:2
- b)2:3
- c)1:1
- d)3:2
- e)2:1
- 【問4】ホルムアルデヒドの他に本実験で生成したアルデヒドの構造式(示性式)を示せ。
- 【問5】下線部②で示した黄色の結晶沈殿物の分子式を記せ。
<東海大学医学部>
解答と解説
<解答>
- 【問1】C4H8
- 【問2】
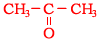
- 【問3】c)
- 【問4】
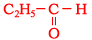
- 【問5】CHI3
<解説>
-
【問1】
化合物中の炭素,水素の割合を求めると
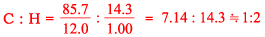 よって組成式はCH2(式量=14.0)である。分子式を(CH2)nとすると臭素が付加した
よって組成式はCH2(式量=14.0)である。分子式を(CH2)nとすると臭素が付加した
(CH2)nBr2の分子量が216になるので
14.0n+160=216
n=4
よって分子式はC4H8 -
【問2】
C4H8で表されるアルケンは幾何異性体を含めて4種類あり,それぞれを酸化すると
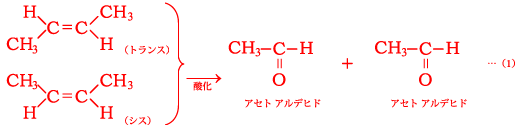
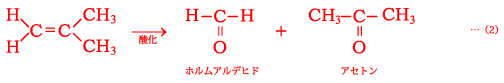
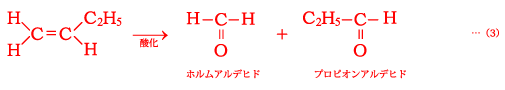 下線部①ではアルデヒドとケトンが生じているので①の反応は(2)の反応であることがわかり,得られるケトンはアセトンと判明する。
下線部①ではアルデヒドとケトンが生じているので①の反応は(2)の反応であることがわかり,得られるケトンはアセトンと判明する。
- 【問3】
(1)~(3)の反応のうちケトンを生成するのは(2)の反応だけなので問題文中の0.50mol生成したケトンはアセトンである。アセトンが0.50mol生成すると(2)の反応でホルムアルデヒドも0.50mol生成する。ホルムアルデヒドは全部で1.0mol生成されているので(3)の反応で0.50molのホルムアルデヒドが生成することがわかる。すると(3)の反応でプロピオンアルデヒドが残りのアルデヒドとして0.50mol生成することがわかる。以上の値から(2)と(3)の反応でA,Bが0.50molずつ反応したことがわかるので,AとBの物質量比は1:1になる。
- 【問4】
問3の解説よりプロピオンアルデヒドが生成したことがわかる。
- 【問5】
アセトンに対するヨードホルム反応で得られた黄色結晶は,ヨードホルムCHI3である。
<補足>
- 1 この問題におけるアルケンの酸化剤としてオゾンが想定できる。(オゾン分解)。
- 2 C4H8酸化の式(1)~(3)を想定したが結局(1)の反応は生じていない。
- 3 酢酸はCH3CO-の構造を持つが,ヨードホルム反応は陰性である。これはCH3CO-にOが結合しているので水素やアルキル基が結合している場合とは反応性が異なるためである。
掟7. アルケンはオゾン分解を受け二重結合が切断されることを常識とすべし。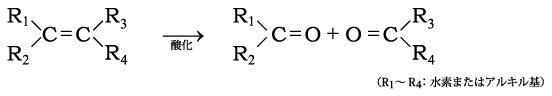
掟8. 有機化学の構造決定の問題ではヨードホルム反応がよく用いられるので,反応に対して陽性の構造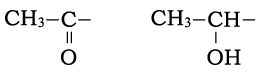 は必ず暗記せよ。また,ヨードホルム反応が陽性のときに生じるヨードホルム(黄色結晶,CHI3)の色や分子式は,よく出題されるので答えられるようにしておくべし。
は必ず暗記せよ。また,ヨードホルム反応が陽性のときに生じるヨードホルム(黄色結晶,CHI3)の色や分子式は,よく出題されるので答えられるようにしておくべし。
注)酢酸は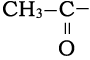 の構造をもつがヨードホルム反応は陰性である。
の構造をもつがヨードホルム反応は陰性である。



