有機化学のオキテ2
問題
C,H,Oからなる,ある芳香族化合物A16.2 mgを,図のようにして元素分析を行ったところ,二酸化炭素が48.4 mg,水が12.6 mg生成していた。また,化合物A 8.10 gをベンゼン100 gに溶かした溶液の凝固点を測定したところ,2.97 ℃であった。なお,ベンゼンの凝固点は5.53 ℃,モル凝固点降下は5.12K・kg/molであり,凝固点降下度は溶液の質量モル濃度に比例するものとする。 C=12.0 H=1.00 O=16.0
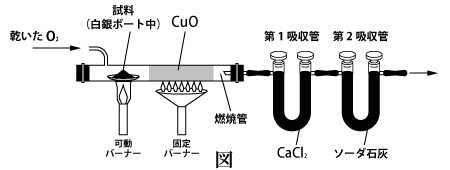

- 【問1】 図の第1吸収管と第2吸収管を逆に接続すると正しい結果が得られない。その理由を30字程度で記せ。
- 【問2】 化合物Aの分子式を示せ。
<東京慈恵会医科大学 一部改>
解答と解説
<解答>
- 【問1】 ソーダ石灰は発生した水と二酸化炭素の両方を吸収するため。(28字)
- 【問2】 C11H14O
<解説>
- 【問1】 逆に接続するとソーダ石灰の入っている吸収管が最初になり,発生したH2OとCO2の両方を吸収してしまい,発生したそれぞれの物質の質量を求めることができない。
-
【問2】 化合物A 16.2 mg中のC,H,Oの質量を求めると
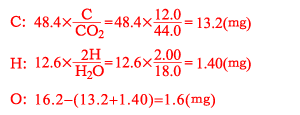
原子数の比は
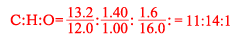
よって化合物Aの組成式はC11H14O(式量162)
化合物Aの分子量Mを求めると⊿t=kmより(⊿t:凝固点降下度,k:モル凝固点降下,m:質量モル濃度)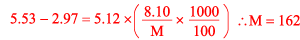 Aの組成式量と分子量が一致するので,Aの分子式はC11H14Oとなる。
Aの組成式量と分子量が一致するので,Aの分子式はC11H14Oとなる。
<補足>
- 1 この問題における計算の手順は決まり切った形式になっているので,その場で考えたりせずに機械的に計算できるようにしておくこと。
- 2 有機化合物の分子量はこの問題のように凝固点降下度から求める場合の他に,気体の状態方程式,浸透圧,中和滴定などから求める場合もある。
掟2. 元素分析の計算は,形式が決まっているので,機械的に計算できるようにしておくべし。



